В периодической системе в одной группе с бором находится химический элемент:
Централизованное тестирование по химии, 2017
В атоме химического элемента 21 электрон. Его относительная атомная масса равна:
Атом ![]() и анион водорода
и анион водорода ![]() в основном состоянии подобны между собой:
в основном состоянии подобны между собой:
Согласно положению в периодической системе наибольшее значение электроотрицательности имеет химический элемент с порядковым номером:
Ковалентная связь имеется во всех веществах ряда:
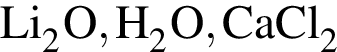
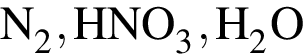
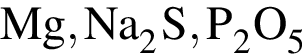
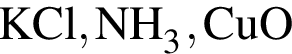
Установите соответствие между формулой вещества и степенью окисления в нем атома химического элемента,указанного в скoбках.
1) Li3N(N)
2) KHS(S)
3) CuSiO3(Si)
a) –3
б) –2
в) –1
г) +4
д) +6
Количество (моль) анионов, содержащихся в 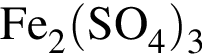 массой 312г, равно:
массой 312г, равно:
С помощью прибора, изображенного на рисунке, способом вытеснения воздуха (Mr=29) с наименьшими потерями можно собрать газ:
Укажите формулу основного оксида:
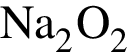
Число веществ среди предложенных - 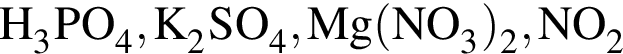 , с которыми реагирует разбавленный водный раствор
, с которыми реагирует разбавленный водный раствор ![]() :
:
Двухосновная бескислородная кислота образуется при взаимодействии в водном растворе веществ:
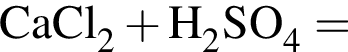
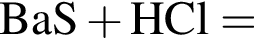
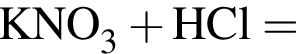
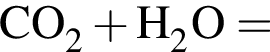
Укажите утверждение, верно характеризующее соль 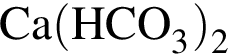 :
:
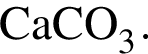
Установите соответствие между веществом и его кристаллической решеткой при н. у.:
1) ромбическая сера
2) бор
3) вода
4) оксид кремния (Ⅳ)
решетка
а) молекулярная
б) атомная
![]() в отличие от
в отличие от ![]() :
:
а — хорошо растворяется в воде
б — относится к сильным кислотам
в — НЕ образует осадок с раствором нитрата ртути(II)
г — НЕ окисляется хлором
Выберите утверждения, верно характеризующие озон:
a) окислительные свойства выражены сильнее, чем у кислорода;
б) является аллотропной модификацией кислорода;
в) молекула состоит из двух атомов;
г) имеет относительную плотность по воздуху менее 1.
Выберите утверждение, верно характеризующее фосфор:
a) в природе встречается в составе апатитов;
б) белый фосфор состоит из молекул ![]() ;
;
в) реагирует с водородом с образованием ![]() ;
;
г) в реакции с магнием является окислителем
Избыток газа, полученного действием серной кислоты на известняк, пропускают в стакан с известковой водой. При этом в стакане:
Железный гвоздь погрузил в разбавленный водный раствор вещества Х. При этом масса гвоздя НЕ изменилась. Веществом Х является:
Укажите верное утверждение относительно 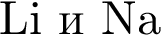 :
:
К раствору серной кислоты добавили алюминий массой 9г. В результате реакции массовая доля кислоты в растворе снизилась от 28% до 14%. Масса(г) исходного раствора:
Образование ![]() из простых веществ протекает по термохимическому уравнению
из простых веществ протекает по термохимическому уравнению 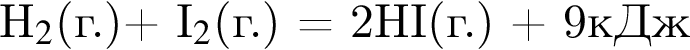 . При разрыве связей в молекулах
. При разрыве связей в молекулах ![]() количеством 1моль поглощается 436кДж теплоты, а при образовании связей в молекулах
количеством 1моль поглощается 436кДж теплоты, а при образовании связей в молекулах ![]() количеством 1моль выделяется 298кДж теплоты. Укажите количество теплоты (кДж), которая поглощается при разрыве связей в молекулах
количеством 1моль выделяется 298кДж теплоты. Укажите количество теплоты (кДж), которая поглощается при разрыве связей в молекулах ![]() количеством 1моль:
количеством 1моль:
Сумма коэффициентов перед веществами НЕмолекулярного строения в уравнении реакции, протекающей по схеме 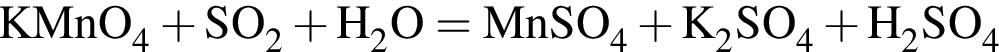 , равна:
, равна:
В водном растворе аммиака установилось следующее равновесие:  . Количество молекул
. Количество молекул ![]() в растворе уменьшится, если добавить в раствор:
в растворе уменьшится, если добавить в раствор:
а) немного твердого гидроксида калия;
б) немного оксида фосфора (V);
в) порцию уксусной кислоты;
г) немного оксида углерода (II).
При охлаждении насыщенного водного раствора ![]() до
до ![]() С в стакане выпал осадок. Укажите правильное утверждение:
С в стакане выпал осадок. Укажите правильное утверждение:
Лампочка прибора для определения электропроводности (см.рис) НЕ изменит яркость,если в разбавленный раствор
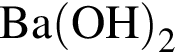 добавить:
добавить:
При добавлении к воде оксида стронция:
а) рН увеличивается;
б) рН уменьшается;
в) концентрация ионов ![]() уменьшается;
уменьшается;
г) концентрация ионов ![]() НЕ изменяется.
НЕ изменяется.
Модель молекулы пропана изображена на рисунке:
Для превращения 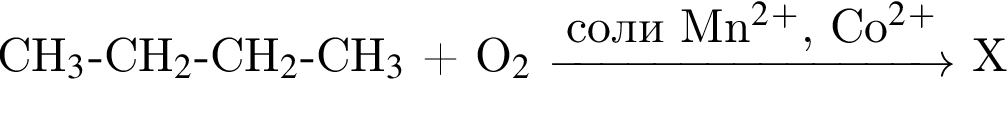 верно:
верно:
Гомологи образуются при гидрировании избытком водорода углеводородов пары:
Дана схема превращений 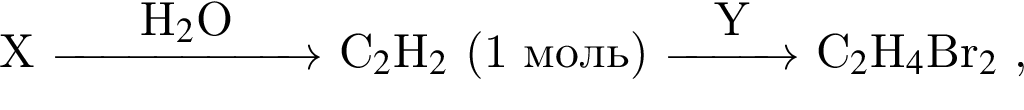 где Х и Y соответственно:
где Х и Y соответственно:
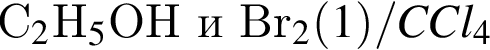
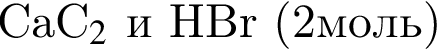
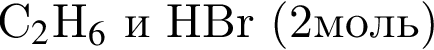
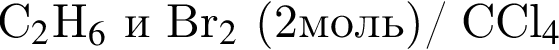
В результате реакции 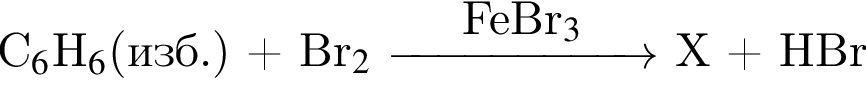
получен бромоводород количеством 0,9 моль. Масса (г) органического продукта Х составляет:
Как глицерин, так и глюкоза:
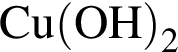
К водному раствору, содержащему фенол массой 36,66г, добавили водный раствор, содержащий гидроксид натрия массой 11,2г. После завершения реакции масса (г) фенола в полученном растворе составляет:
Строение карбоксильной группы верно отражено на рисунке:
В качестве моющего средства можно использовать вещество, формула которого:
Укажите верное утверждение относительно сахарозы:
Число пептидных связей в молекуле
равно:
Мономером для получения полимера является вещество:
Альдегид А имеет молярную массу меньше 45 г/моль. При гидрировании А образуется вещество Б с молярной массой больше 45 г/моль. При окислении А перманганатом калия в кислой среде может быть получено органическое вещество В, водный раствор которого окрашивает лакмус в красный цвет. При нагревании Б с В в присутствии серной кислоты получается легкокипящая жидкость Г и неорганическое вещество Д. Найдите сумму молярных масс (г/моль) веществ В и Г.
Выберите утверждения, верно характеризующие олеиновую кислоту.
| 1 | В молекуле содержится 18 атомов углерода |
| 2 | Имеет структурную формулу Н3С – (СН2)7 – СН=СН – (СН2)7 – СООН |
| 3 | В реакции с водородом образует пальмитиновую кислоту |
| 4 | При взаимодействии с бромом получается вещество С17Н33Вr2СООН |
| 5 | Получают в результате гидролиза соединения |
| 6 | Хорошо растворяется в воде |
Ответ запишите в виде последовательности цифр в порядке возрастания, например: 245 .
Газообразная смесь алкана с этеном имеет объем (н. у.) 13,44дм3. Половину смеси пропустили через сосуд с избытком бромной воды. При этом масса сосуда с содержимым выросла на 3,5г. Вторую половину смеси сожгли в избытке кислорода, в результате чего образовалась вода массой 10,8 г. Определите молярную массу (г/моль) смеси углеводородов.
Определите сумму молярных масс (г/моль) азотсодержащих веществ А и Б, полученных в результате следующих превращений:
Дан перечень неорганических веществ: аммиачная селитра, графит, гидросульфит натрия, гидроксид железа(II), кремнезем, карбонат калия, оксид лития, фтор. Укажите число нерастворимых оснований, солей, высших оксидов и простых веществ соответственно.
Ответ запишите цифрами, соблюдая полученную последовательность, например: 2231.
Простое газообразное вещество А желто-зеленого цвета с резким запахом реагирует с металлом Б, в результате чего получается вещество В. Газ А имеет плотность (н. у.), равную 3,17г/дм3. Химический элемент, образующий Б, в соединениях имеет валентность II, а избыток его катионов обуславливает жесткость воды. При действии на В массой 33,84г избытка концентрированной серной кислоты с выходом 82% выделяется бесцветный, хорошо растворимый в воде газ Г объемом (н. у.) 11,2дм3. Определите сумму молярных масс (г/моль) веществ А и В.
Для получения веществ по схеме превращений:
![]() →
→![]() →
→ 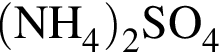 →
→ 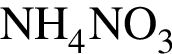 →
→ ![]()
выберите варианты из предложенных:
1 - 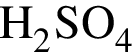
2 - 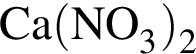
3 - ![]()
4 - 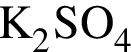
5 - ![]()
6 - 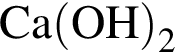
Ответ запишите цифрами в порядке следования превращений, например, 5314.
В четырех пронумерованных пробирках находятся разбавленные растворы неорганических веществ. О них известно следующее:
- раствор из пробирки 2 нейтрализуется раствором из пробирки 3;
- растворы из пробирок 1 и 2 реагируют между собой с образованием осадка, который растворяется как в кислотах, так и в щелочах;
- при добавлении к содержимому пробирки 3 вещества из пробирки 4 выделяется бесцветный газ.
Установите соответствие между названием вещества и номером пробирки, в котором находится раствор данного вещества.
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например, А1Б4В3Г2.
Уксусная кислота широко применяется в качестве консерванта (пищевая добавка Е260). В быту чаще всего используют уксус (массовая доля кислоты 9%, 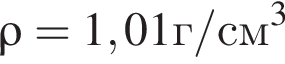 ) или уксусную эссенцию (массовая доля кислоты 70%,
) или уксусную эссенцию (массовая доля кислоты 70%,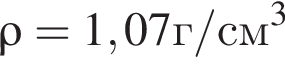 ). Для консервирования овощей требуется 250см3 уксуса. Вычислите, в каком объеме воды (см3) необходимо растворить уксусную эссенцию, чтобы приготовить раствор для консервирования.
). Для консервирования овощей требуется 250см3 уксуса. Вычислите, в каком объеме воды (см3) необходимо растворить уксусную эссенцию, чтобы приготовить раствор для консервирования.
Найдите сумму молярных масс (г/моль) алюминийсодержащих веществ Б и Д,образовавшихся в результате следующих превращений:
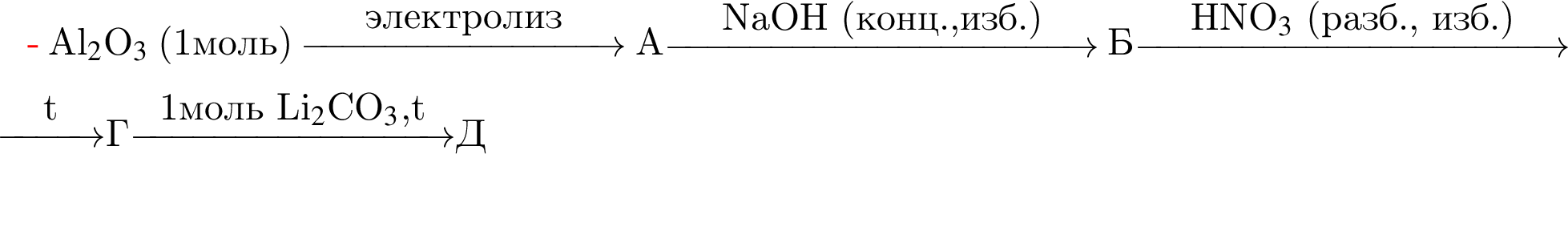
В результате поджигания смеси объемом (н. у.) 500дм3, состоящей из сероводорода, взятого в избытке, и кислорода, образовались сера и вода. После приведения полученной смеси к нормальным условиям в газообразном состоянии остался только сероводород объемом 200дм3. Рассчитайте объемную долю (%) кислорода в исходной смеси.
Для анализов смеси хлоридов калия и аммония провели следующие операции. Навеску смеси массой 10г растворили в воде. К полученному раствору прибавили 540г раствора гидроксида калия с массовой долей ![]() 2,8% и нагрели до полного удаления аммиака. В образовавшийся раствор добавили метиловый оранжевый, а затем акуратно прибавляли соляную кислоту, пока среда раствора не стала нейтральной. Объем израсходованной кислоты равен 330см3, концентрация HCl в кислоте 0,5моль/дм3. Вычислите массовую долю(%) хлорида аммония в исходной смеси.
2,8% и нагрели до полного удаления аммиака. В образовавшийся раствор добавили метиловый оранжевый, а затем акуратно прибавляли соляную кислоту, пока среда раствора не стала нейтральной. Объем израсходованной кислоты равен 330см3, концентрация HCl в кислоте 0,5моль/дм3. Вычислите массовую долю(%) хлорида аммония в исходной смеси.

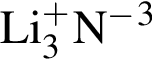
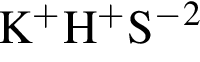
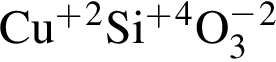
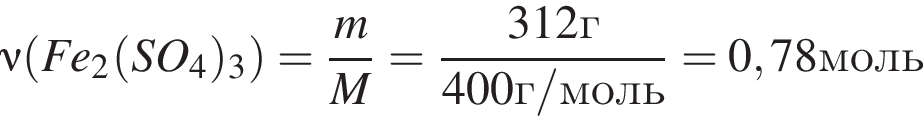
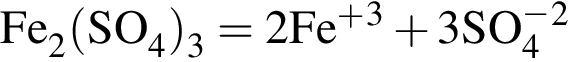
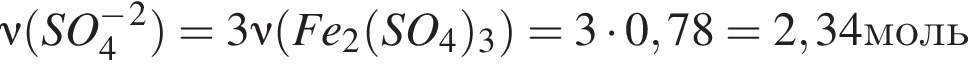
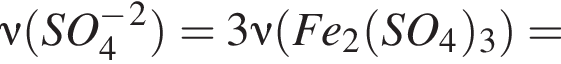

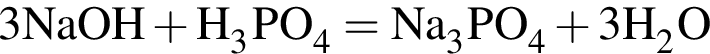
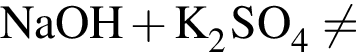
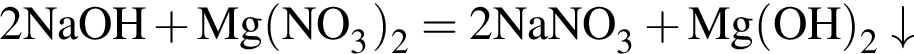
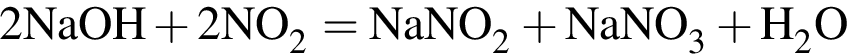
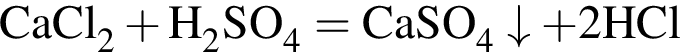
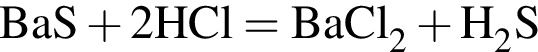
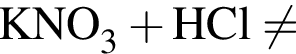
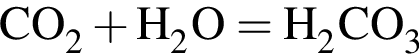
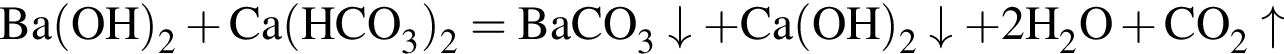
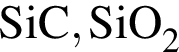 .
.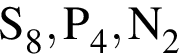 .
.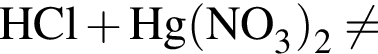
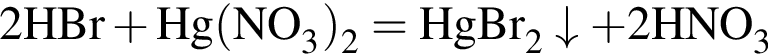
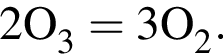
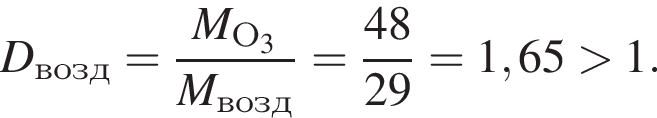
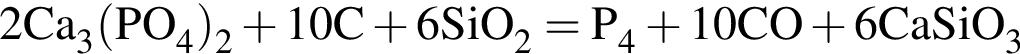
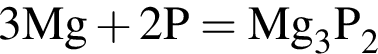 ;
; 
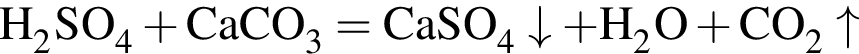
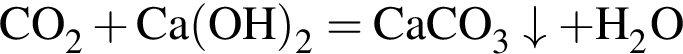
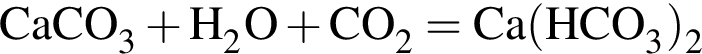
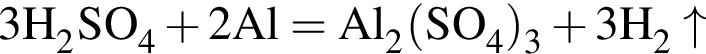
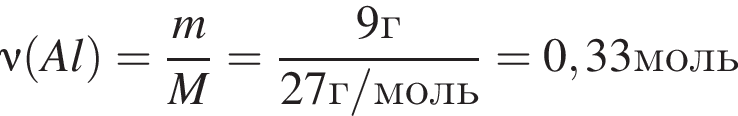
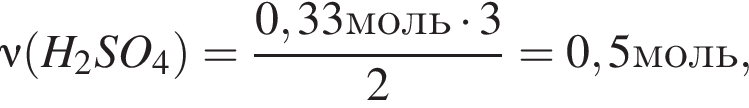 откуда
откуда 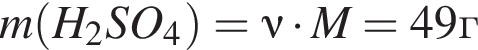 и
и 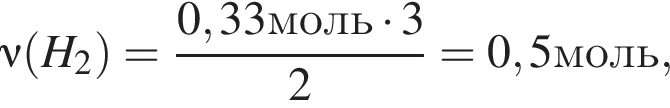 откуда
откуда 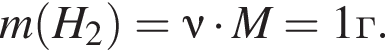
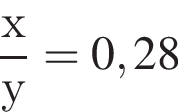
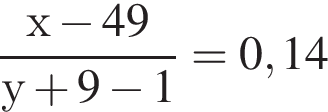
 т. е.
т. е.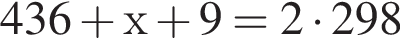
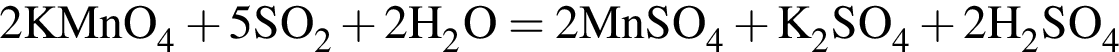
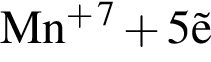 →
→ 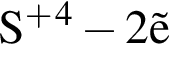 →
→ 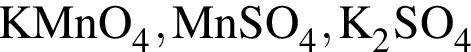 - вещества ионного строения,
- вещества ионного строения,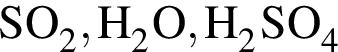 - вещества молекулярного строения.
- вещества молекулярного строения.
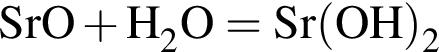
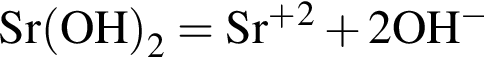
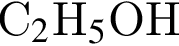 - этанолу (1),
- этанолу (1), 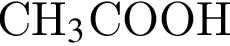 - уксусной кислоте (2),
- уксусной кислоте (2), 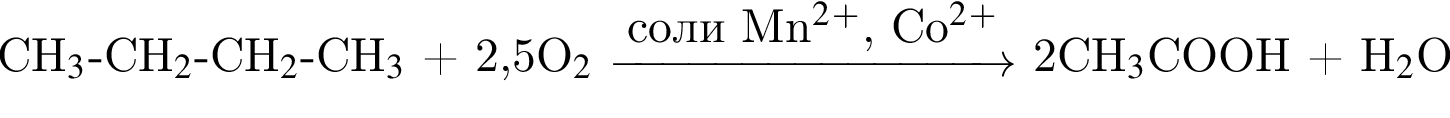
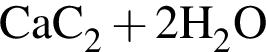 →
→ 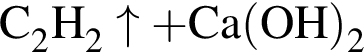
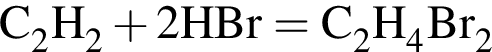
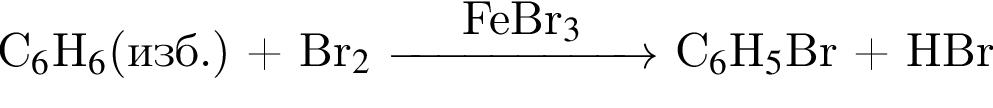
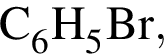 учитывая стехиометрические коэффициенты уравнения реакции, очевидно, что:
учитывая стехиометрические коэффициенты уравнения реакции, очевидно, что:

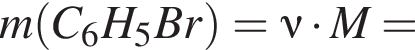
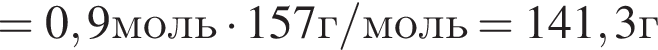
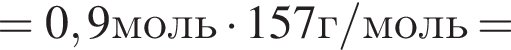
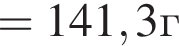
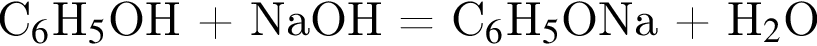
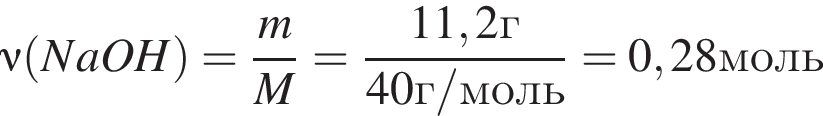
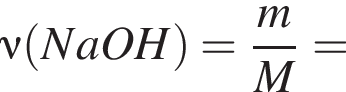
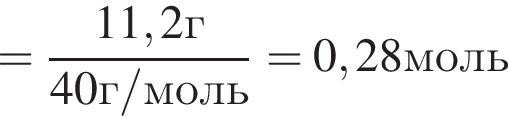
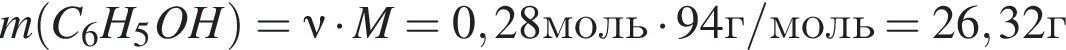

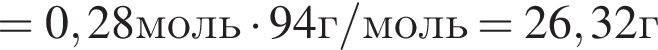
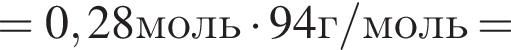
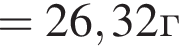
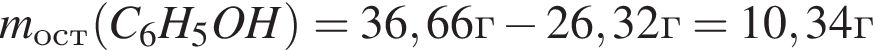

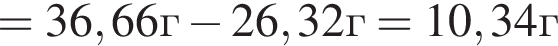
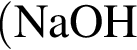 в твердых мылах,
в твердых мылах, 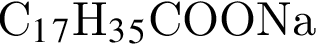 .
.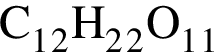 (т. к. сахароза - дисахарид, состоящий из двух моносахаридов - фруктозы
(т. к. сахароза - дисахарид, состоящий из двух моносахаридов - фруктозы 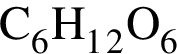 и глюкозы
и глюкозы 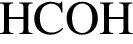 (Mr=30 г/моль) и
(Mr=30 г/моль) и 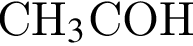 (Mr=44 г/моль). Прогидрируем их:
(Mr=44 г/моль). Прогидрируем их: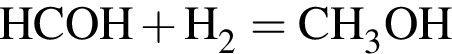
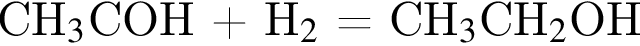
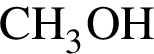 )= 32 г/моль, что меньше 45г/моль,
)= 32 г/моль, что меньше 45г/моль,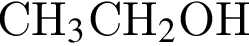 )= 46 г/моль, что больше 45г/моль. Следовательно, А -
)= 46 г/моль, что больше 45г/моль. Следовательно, А - 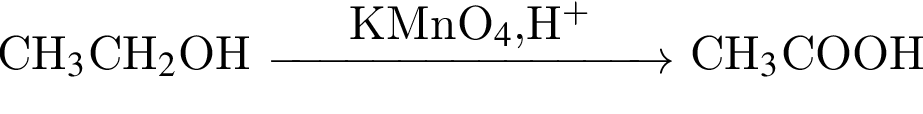 . В -
. В - 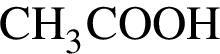 , которая окрашивает лакмус в красный цвет.
, которая окрашивает лакмус в красный цвет. 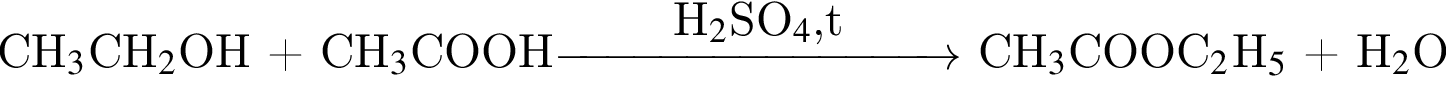 , где Г -
, где Г - 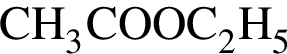 , а Д -
, а Д - 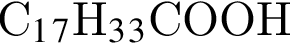 . Очевидно, что у нее 18 атомов углерода.
. Очевидно, что у нее 18 атомов углерода.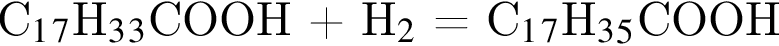 Формула пальмитиновой кислоты -
Формула пальмитиновой кислоты - 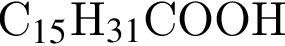 .
.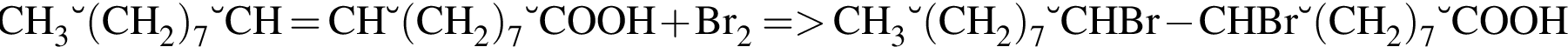 , что соответствует
, что соответствует 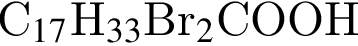
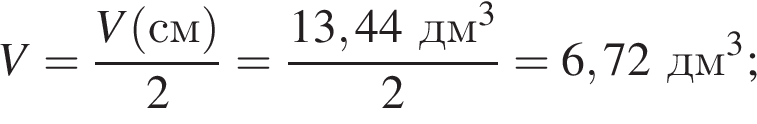

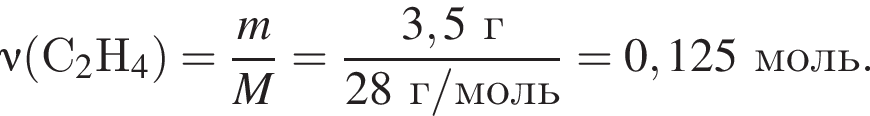
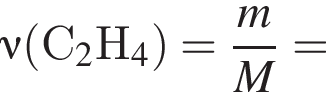
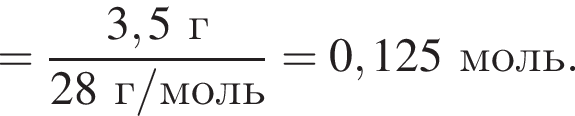
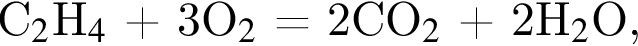
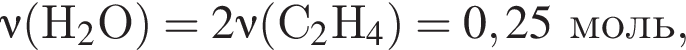

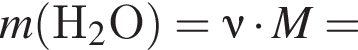
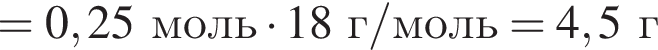
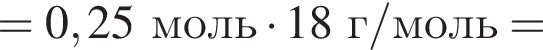
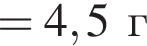
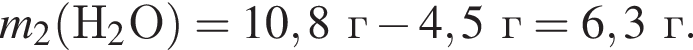
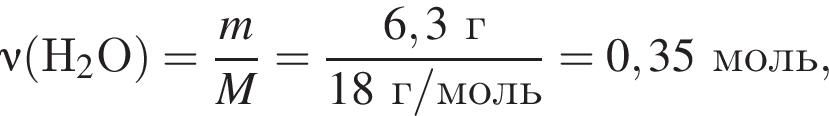
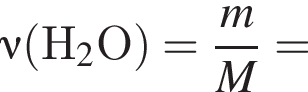
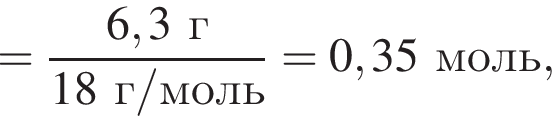

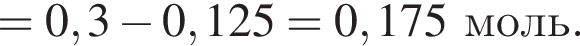
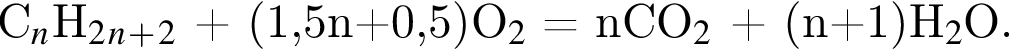
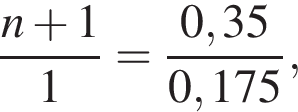 откуда n = 1, следовательно, это метан.
откуда n = 1, следовательно, это метан.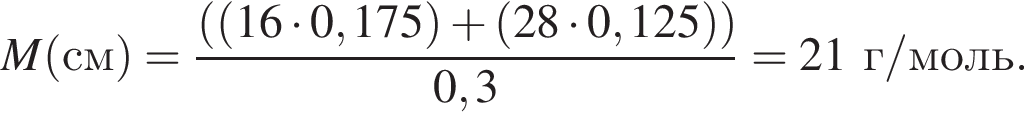
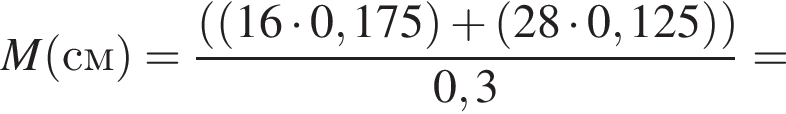
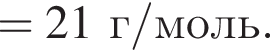

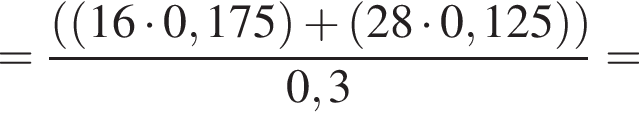
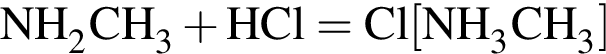
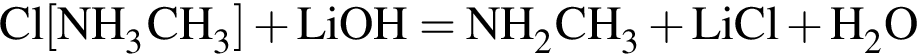
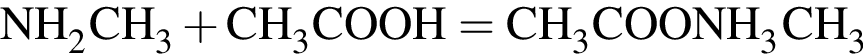
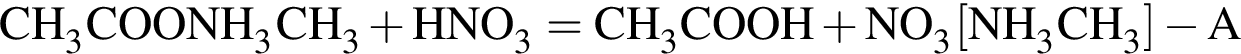
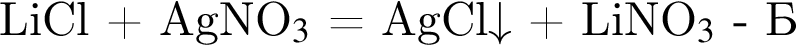
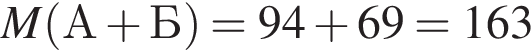
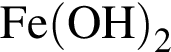 ;
;
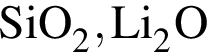 ;
;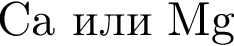 , т. к. они оба в соединениях имеют валентность II, а избыток их катионов обуславливает жесткость воды.
, т. к. они оба в соединениях имеют валентность II, а избыток их катионов обуславливает жесткость воды. 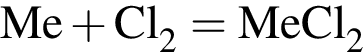 , где
, где 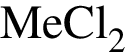 - вещество В.
- вещество В.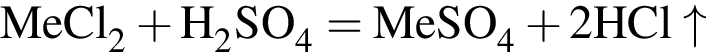 , где
, где 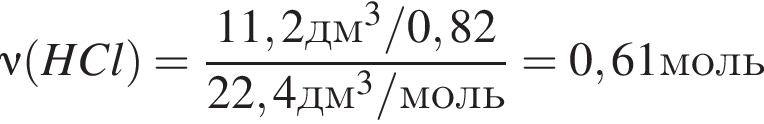
 Откуда
Откуда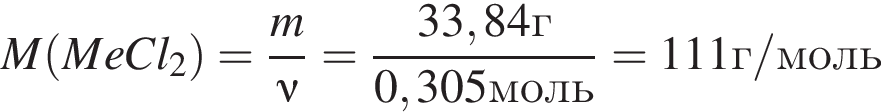

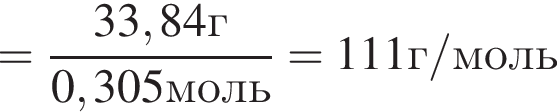

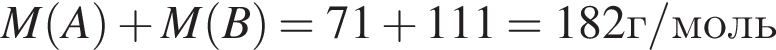
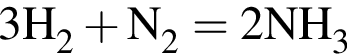
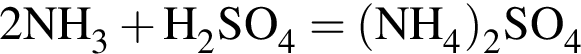
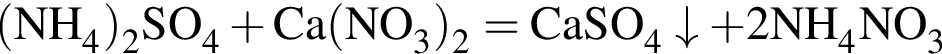
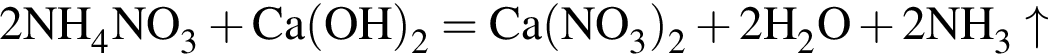
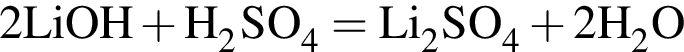 - реакция нейтрализации.
- реакция нейтрализации. 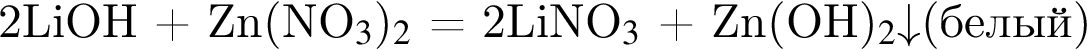
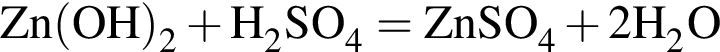 ,
,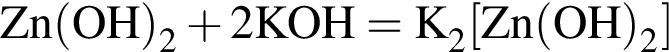 .
.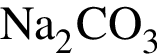 :
: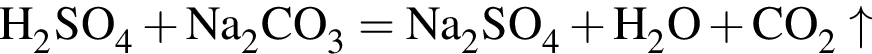 - бесцветный газ.
- бесцветный газ. 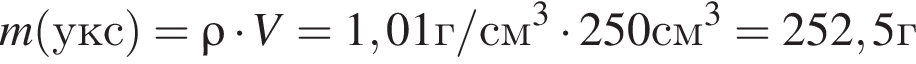


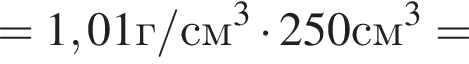

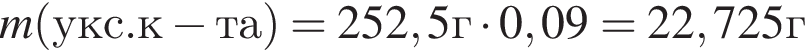
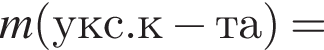

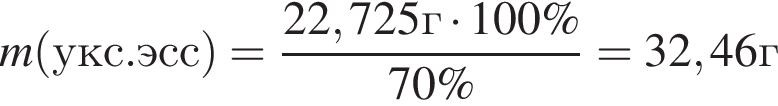
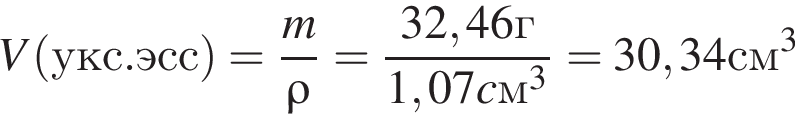
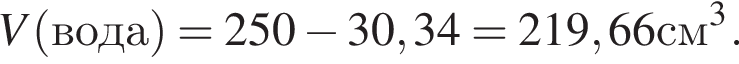 Округлив до целых, получим 220см3.
Округлив до целых, получим 220см3.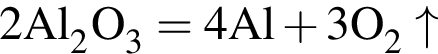
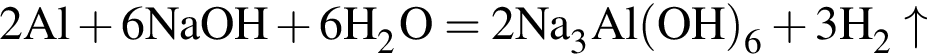
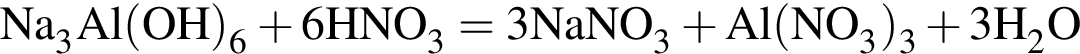
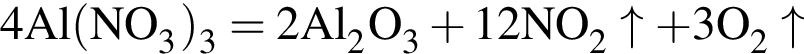
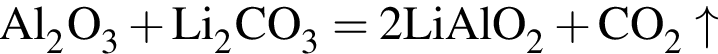
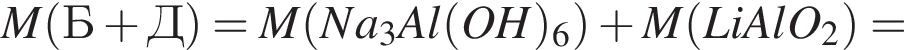


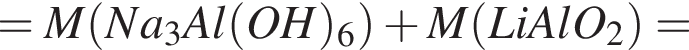
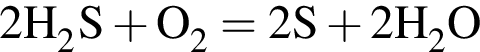
 т. е. V(
т. е. V(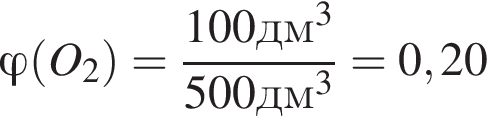 (20%).
(20%).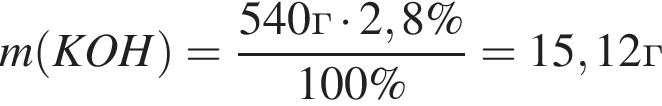
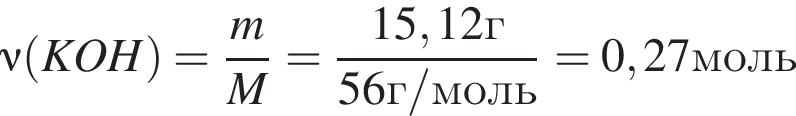
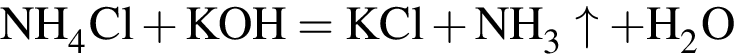 , оставшийся
, оставшийся 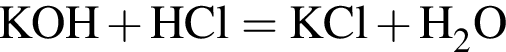
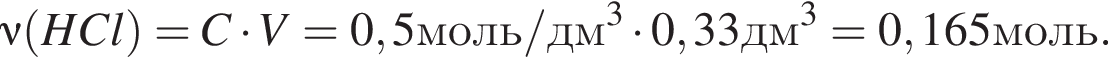

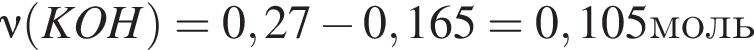 прореагировало с
прореагировало с 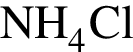 .
. Найдем массу хлорида аммония:
Найдем массу хлорида аммония: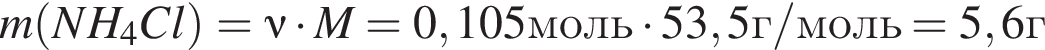

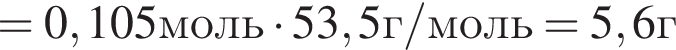
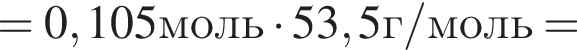
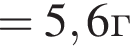
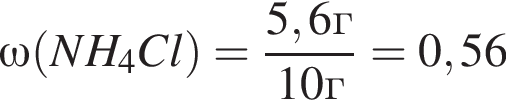 (56%)
(56%)